- サービス

- 業界

- リソース

- 会社概要

業務内容ホーム
生成 AI
- AI 翻訳サービス
- Content Remix
AI トレーニング
- Aurora AI Studio™
機械翻訳
- MT トラッカー
Smart Onboarding
翻訳サービス モデル
コンテンツ サービス
- テクニカル ライティング
- トレーニング/eラーニング
- 財務報告書
- デジタル マーケティング
- SEO/コンテンツ最適化
翻訳サービス
- 動画ローカリゼーション
- ソフトウェア ローカリゼーション
- Web サイト ローカリゼーション
- 規制対象企業向け翻訳
- 通訳
- ライブ イベント
- 言語品質サービス
テスティング サービス
- 機能 QA/テスト
- 互換性テスト
- 相互運用性テスト
- パフォーマンス テスト
- アクセシビリティ テスト
- UX/CX テスティング
インサイト
- ブログ記事
- ケース スタディ
- ホワイトペーパー
- ソリューション概要
- インフォグラフィック
- eBook
- 動画
ウェビナー
ライオンブリッジのナレッジ ハブ
- 良好な患者アウトカム
- 最新の臨床試験ソリューション
- 患者エンゲージメント
- AI のソート リーダーシップ
言語を選択:
EU における規制関連翻訳のニーズの特定
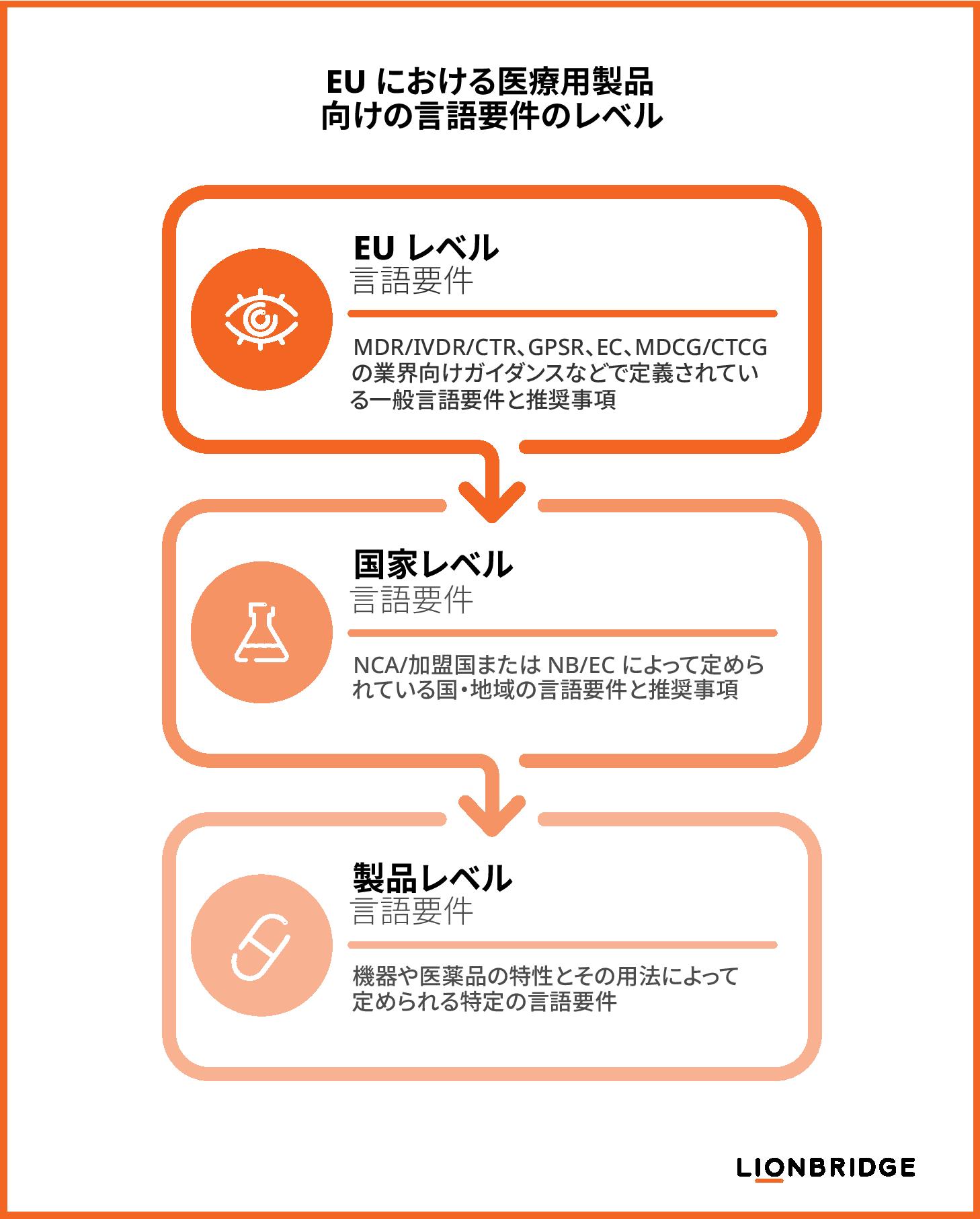
EU の医療機器規則および臨床試験に関する規則により、医療機器メーカーまたは臨床試験依頼者は、次の 3 つのレベルの言語要件を考慮して、ライフ サイエンス分野の規制に確実に準拠する必要があります。
EU レベルの要件: MDR/IVDR/CTR、一般製品安全規則 (GPSR)、欧州委員会 (EC) の発行物、および医療機器調整グループ (MDCG) や臨床試験調整グループ (CTCG) が発行した業界向けガイダンス ドキュメントで定義されています。
国家レベルの要件: 各加盟国の所轄官庁 (NCA) によって決定され、一部は適合性評価機関 (NB) により医療機器の適合性評価手順の一環として、または倫理委員会 (EC) により臨床試験承認手続きの一環として施行されます。
製品レベルの要件: 使用状況、製品特性、対象ユーザーや用途など、製品に関する具体的な考慮事項によって決定されます。
ライフ サイエンス分野の規制準拠に向けた EU レベルの言語要件
EU レベルの言語要件は一般的なものです。基本的に、EU 内で出荷されるすべての消費者製品は、一般製品安全規則 (GPSR) の対象となります。GPSR では、製品が提供される加盟国の定めに従い、以下の情報および文書をその国の公用語で作成することが義務付けられています。
- 使用説明書
- ラベル情報
- 消費者製品用ドキュメント
医療機器や医薬品など、安全性や性能に関して追加的な要件が求められる製品の場合、言語要件の適用対象は製品に付属するラベルや情報だけにとどまりません。たとえば医療機器メーカーは、簡潔な言葉、平易な表現、あるいは現地の言語を使って機器の安全性や性能をサポートする責任があります。EU レベルの言語要件では、各加盟国について、どの公用語を使用する必要があるかまでは定められていません。
国家レベルの言語要件
それぞれの市場における医療機器や医薬品の各種情報に必要な具体的な言語は、各加盟国の所轄官庁 (NCA) が決定します。一般的に、患者向けのあらゆるコンテンツは、患者の安全を確保するために各加盟国の現地語で提供する必要があります。さらに加盟国の規制当局は、以下のように、コミュニケーションのその他の側面についても検討します。
- 読み手のリテラシー レベル
- 技術的・医学的知識
- トレーニング
EU の NCA では、英語を共通言語とみなすかどうか、また専門的ユーザー向けのコンテンツは英語でよいかどうかに関して、意見が分かれています。フランスやイタリアなど一部の加盟国に加え、ブルガリア、ハンガリー、リトアニアなど東欧の多くの加盟国では、以下のコンテンツは現地語で提供しなければなりません。
- マーケティング資料
- 現場の安全に関する通知
- 認証
北欧の加盟国デンマークやスウェーデンなど、他のいくつかの国々では、英語は例外措置として認められています。
製品レベルの言語要件
製品レベルの要件の対象には、特定の機器や医薬品に固有のユース ケースが含まれます。たとえば、自己検査やベッドサイド検査を目的とした体外診断用医療機器や、患者データの取得に使用されるモバイル アプリケーションなどです。
EU レベルや国家レベルの発行物で十分に指定されていない場合は、メーカーが機器や医薬品の具体的な使用状況を考慮して、言語に関するニーズを判断する必要があります。当社のグローバル規制ソリューションの専門家は、不明点がある場合、機器や医薬品を市場に出したり臨床試験を実施したりする前に、適合性評価機関または各加盟国の所轄官庁に相談することを推奨しています。
言語によるアクセス性、安全性、透明性の確保
医療機器メーカーおよび臨床試験依頼者が EU 市場に参入するには、ライフ サイエンス分野の規制と言語要件を確実に遵守しなければなりません。言語要件に対処するということは単純な作業ではなく、情報を EU の各現地語で提供することで、すべての製品ユーザーと試験ボランティアにとって情報をアクセスしやすく、わかりやすく、透明性のあるものにする必要があります。さらに、高品質の翻訳ときめ細かな文化的ニュアンスへの対応を通じて、メーカーは市場での存在感を高められると同時に、製品が安全に使用されることをより確実にできます。
お問い合わせ
EU 市場の規制への言語面の対応について支援をお求めであれば、ライオンブリッジが提供する EU 規制対応の各種翻訳ソリューションをご検討ください。当社は医療機器や医薬品に関する EU の規制と言語要件について数十年に及ぶ経験を持ち、製品開発のあらゆる段階を支援するライフ サイエンス分野に特化した翻訳・言語サービスを通じて、多くのお客様をサポートしています。
お問い合わせフォームにて当社までご相談ください。
ライオンブリッジでは、お客様のニーズをより深く理解し、課題を解決して海外市場へのリーチ拡大をお手伝いするうえで、当社の革新的な技術がどのように役立つかを詳しくお伝えしたいと考えています。これらの技術の活用についてご興味があれば、ぜひ当社までお問い合わせください。