- 我们的服务范围

- 行业

- 资源

- 公司简介

选择语言:
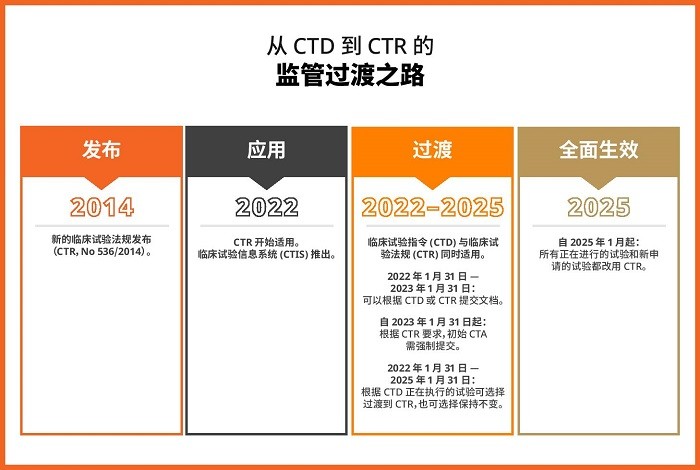
从困局走向卓越
CTR 的实施旨在促进欧盟的跨国临床研究。尽管改革伴随着一些短期困扰与压力,但其背后却承载着一项宏伟愿景,即在欧盟范围内实现临床试验要求的协调统一与执行过程的显著优化。随着 CTIS 的实施,欧盟的临床试验申请程序将变得更加高效。此外,还可能存在针对所有相关成员国的单一提交和联合评估的情况。新程序可将标准的 60 天缩短到 45 天(未计入信息请求的延期时间)。
此外,欧盟从 CTD 到 CTR 的法律过渡,使得各成员国之间的技术要求得到了协调一致。这有望使试验审批与执行变得更为高效,令申办者、患者和监管机构都能从中受益。CTIS 的公共界面还将进一步提升区域临床研究的透明度,使患者与潜在试验参与者能够便捷地获取区域临床试验的相关信息。
根据欧洲药品管理局 (EMA) 的描述,CTR 的目标是:
“...促进欧盟的创新与科研进展,为在多个欧盟成员国/欧洲经济区 (EEA) 国家顺利开展大规模临床试验创造有利条件。”
根据 EMA 的描述,CTIS 的好处包括:
- “允许申办者通过一份在线申请来申请多达 30 个欧洲国家/地区的临床试验授权;
- 使各国监管机构能够协同处理多个国家/地区的临床试验申请,要求提供更多资料,批准或拒绝试验,并监督已授权的试验;
- 便于试验扩展至其他 EEA 国家;
- 通过可搜索的公开网站,使对 EEA 内进行的临床试验感兴趣的任何各方都能获取透明信息和访问权限。”
跨国试验平均涉及六个成员国
自 2022 年上线以来,CTIS 已收到 3,657 份临床试验申请 (CTA)。仅在 2024 年 1 月,就有 309 份 CTA 提交到该系统。其中,有 170 份为首次提交的 CTA,商业临床试验中跨国试验的比例最高。截至 2024 年 1 月,共有 1,144 项跨国试验在 CTIS 中收到申请结果;这些试验平均涉及六个成员国。所有这些试验均须使用各欧盟成员国的当地官方语言翻译所需的提交资料内容。自 2022 年 1 月以来首次提交的跨国试验的 CTA 分布情况如下图所示。

AI 解决方案:扩展和提速需要 AI 赋能的语言策略
如果 CTR 成功吸引更大规模的临床试验进入欧盟,语言工作将愈发加重临床试验预算压力,同时也将给负责临床试验申请及当地审校 (ICR) 的临床试验工作人员带来负担。此外,在试验准备阶段需要对语言事务进行细致规划,以确保各语言版本能支持:
- 通过 CTIS 同步提交
- 在短暂的监管审查窗口期内进行的任何更新
该系统基于默示决策原则。这表示,如果申办者未能在成员国当局信息请求的截止日期前作出回应,申请将针对所有相关成员国失效。
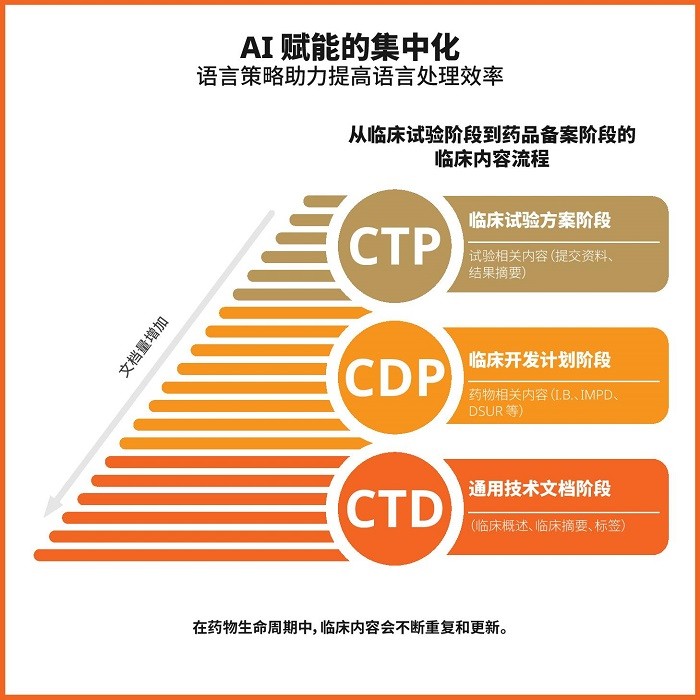
大型语言模型 (LLM) 和生命科学 AI 服务有望大幅加快临床试验的翻译进程,同时确保大量内容的语言一致性。值得注意的是,LLM 的输出质量正在迅速提升。试验申办者在采取有力的语言策略的基础上,结合采用设定有不同人工介入程度的 LLM,可以充分利用 AI 解决方案的优势。(二者同时仍将帮助降低风险。)此类策略可按下图所示在多个级别进行设计。
联系我们
是否需要协助来制定生命科学翻译策略?是否想要详细探索生命科学领域的 AI 解决方案?Lionbridge 在临床试验翻译方面积累了数十年的深厚知识和专业经验。欢迎立即与我们联系,了解 Lionbridge 作为生命科学语言服务提供商的更多信息。





